تازه های بیوتکنولوژی
جدیدترین دستاوردهای بیوتکنولوژی، نانوبیوتکنولوژی و بیوانفورماتیک
تازه های بیوتکنولوژی
جدیدترین دستاوردهای بیوتکنولوژی، نانوبیوتکنولوژی و بیوانفورماتیکواکنش زنجیره ای پلیمراز (PCR)
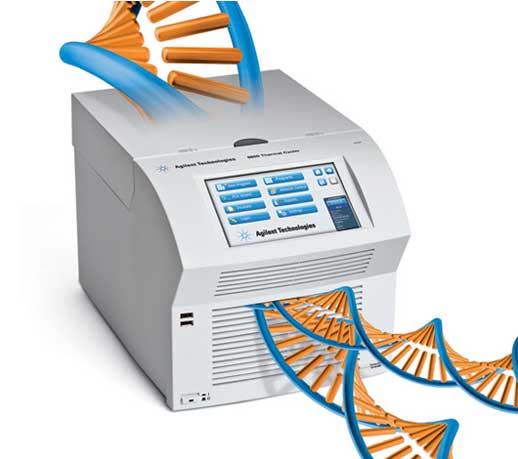
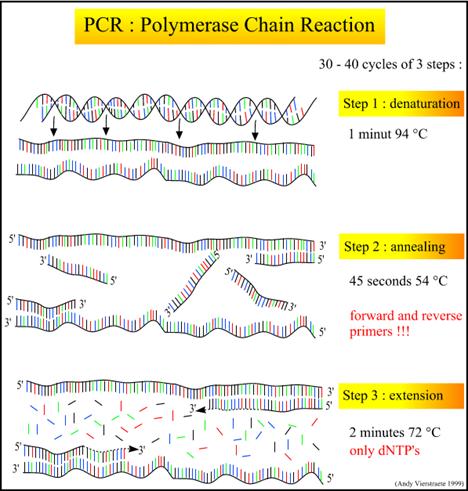
در بیولوژی مولکولی، واکنش زنجیره ای پلیمراز یا PCR، بمنظور تکثیر یک قطعه DNA مورد استفاده قرار میگیرد. تکنیک PCR در سال 1984 توسط کری مولیس (Kary Mullis) ارائه شده است. در این تکنیک، یک مولکول DNA میلیونها بار تکثیر میشود. در روش PCR سیکل های دمایی (Cycle) ایجاد میشود. در ابتدا با ایجاد حرارت و رساندن دمای محلول به نقطه ذوب DNA، دو رشته DNA از هم جدا میشوند. در مرحله بعد با کاهش دما یک آنزیم DNA پلیمراز فعال شده، عمل همانند سازی (Replication) را انجام میدهد. DNA پلیمراز آنزیمی است که با استفاده از نوکلئوتیدها (مصالح ساختمانیDNA)، رشته الگو(DNAی مورد مطالعه) و یک قطعه پرایمر قادر به همانند سازی است. صحت نتایج PCR بستگی به انتخاب پرایمر مناسب دارد. پرایمرها قطعات کوچک پلی نوکلئوتیدی هستند و در آزمایشگاه به گونه ای طراحی و سنتز شده اند که دارای سکانس نوکلئوتیدی مکمل با ناحیه َ3 در مولکول DNAی مورد نظر هستند. بنابر این بطور اختصاصی فقط به این مولکولها متصل شوند. چون آنزیم DNA پلیمراز به قطعات پرایمر متصل میشود، در نتیجه فقط مولکول DNAی هدف همانند سازی و تکثیر میگردد. با اعمال تغییرات دمایی بطور متوالی و برنامه ریزی شده، روند PCR تکرار گردیده و در هر مرحله DNA دو برابر میشود. بنابر این تعداد مولکولهای DNA بصورت تصاعدی و به نسبت n2 افزایش می یابد که n تعداد سیکل های دمایی است. مثلا یک مولکول DNA، پس از 20 سیکل به 1.047.586 مولکول تکثیر میشود. در مرحله همانند سازی، برای جدا نگهداشتن دو رشته DNA، باید دمای محلول بالا باشد. بنابر این از یک نوع آنزیم DNA پلیمراز مقاوم به حرارت استفاده میشود. اولین آنزیمی که بدین منظور مورد استفاده قرار گرفت Taq polymerase بود که از باکتری ترموس آکواتیکوس(Thermus aquaticus) بدست می آید.
امروزه PCR بعنوان یک ابزار مهم در فعالیتهای تحقیقاتی و بالینی محسوب میشود. بعضی از کاربردهای PCR عبارتند از: کلونینگ DNA بمنظور تعیین توالی، فیلوژنی بر اساس DNA (آنالیزعملکردی ژنها)، تشخیص بیماریهای ارثی، انگشت نگاری ژنتیکی (در تعیین والدین و جرم شناسی) و تشخیص بیماریهای عفونی. در سال 1993 به پاس ابداع تکنیک PCR، جایزه نوبل به کری مولیس اهداء گردید.
PCR برای تکثیر بخشهای خاصی از مولکول DNA مورد استفاده قرار میگیرد. این بخشها ممکن است یک ژن کامل، قسمتی از یک ژن یا سکانسهای بین ژنها باشند. در بسیاری از روشهای PCR، قطعات DNAی هدف حداکثر 10 کیلو جفت باز(kb) دارند. اگرچه در بعضی از روشهای خاص، قطعات بزرگتر حتی تا kb40 را هم میتوان تکثیر کرد. محلول PCR معمولا حاوی مواد زیر است:
1. DNAی الگو: شامل DNAی هدف است که تکثیر میگردد.
2. پرایمرهای Forward و Reverse: به گونه ای طراحی شده اند که هر یک مکمل ناحیه َ3 در یکی از رشته های DNA باشد.
3. Taq polymerase یا DNA پلیمراز دیگری که دمای بهینه اش در حدود 70 درجه سانتیگراد باشد.
4. دزوکسی نوکلئوزید تری فسفاتها (dNTPs): مصالح ساختمانی که توسط DNA پلیمراز برای ساختن رشته های DNAی جدید بکار میروند.
5. محلول بافر: شرایط محیطی مناسبی را از نظر pH و یونهای مختلف ایجاد میکند تا پایداری DNA پلیمراز و فعالیت بهینه آن تامین شود.
6. کاتیونهای دو ظرفیتی: یونهای منیزیم یا منگنز
7. کاتیون یک ظرفیتی: یون پتاسیم
محلولPCR معمولا به حجم 10 تا 200 میکرولیتر در لوله های کوچک 0.2 تا 0.5 میلی لیتر تهیه میشود. این لوله هل در بلوکهای مخصوصی در دستگاه ترموسایکلر قرار داده میشوند. ترمو سایکلر، طبق برنامه ریزی انجام شده، دمای لوله ها را در زمانهای مشخصی افزایش و کاهش میدهد تا مراحل مختلف PCR انجام شود. برای جلوگیری از تبخیر محلول (و در نتیجه افزایش غلظت در بخشهای بالائی محلول)، معمولا یک لایه روغن بر سطح محلول قرار داده مبشود. ولی در دستگاه های جدیدتر از درپوش های حرارتی استفاده میشود.
در روش PCR تغییرات دمائی(سیکل ها) بین 20 تا 40 بار تکرار میشود. تعداد سیکل ها با توجه به مقدار DNAی اولیه، شرایط آزمایش و مقدار محصول مورد نیاز انتخاب میشود. دمای لوله ها و فواصل زمانی هم تابع عوامل مختلفی است از جمله: نقطه ذوب پرایمرها (Tm)، نوع DNA پلیمراز، غلظت یونهای دو ظرفیتی و غلظت dNTPها.
مراحل PCR:
1. مرحله شروع (Initialization step): به مدت 1 تا 9 دقیقه دمای محلول به 94 تا 96 درجه (یا 98 درجه اگر پلیمرازها کاملا به حرارت مقاوم باشند) رسانیده میشود. این مرحله فقط برای DNA پلیمرازهایی ضروری است که نیازمند فعال شدن توسط حرارت در روشhot-start PCR هستند.
2. مرحله واسرشت (Denaturation step): این مرحله اولین قسمت از سیکل های حرارتی منظم است و شامل حرارت دادن محلول به مدت 20 تا 30 ثانیه در دمای 94 تا 98 درجه است. در این مرحله بعلت گسستن پیوندهای هیدروژنی (بین نوکلئوتیدها)، DNAی الگو و پرایمرها از هم جدا میشوند و تک رشته های DNA حاصل میگردد.
3. مرحله اتصال (Annealing step): دمای محلول به مدت 20 تا 40 ثانیه به 50 تا 65 درجه کاهش می یابد. در این مرحله پرایمرها به تک رشتهای DNAی الگو متصل میشوند. بطور طبیعی، دمای اتصال (Annealing temperature) در حدود 3 الی 5 درجه پائین تر از نقطه ذوب پرایمرها است. پیوندهای هیدروژنی پایدار فقط زمانی شکل میگیرد که سکانس پرایمر و رشته الگو مکمل یکدیگر باشند. آنزیم پلیمراز پس از اتصال به هیبرید پرایمر-الگو، همانند سازی DNA را آغاز میکند.
4. مرحله طویل شدن (Extension/elongation step): دمای محلول در این مرحله باید متناسب با نوع DNA پلیمراز مورد استفاده باشد. دمای اپتیمم برای آنزیم Taq polymerase حدود 75 الی 80 درجه است که معمولا دمای 72 درجه انتخاب میشود. در این مرحله آنزیمDNA پلیمراز با استفاده از dNTP های موجود در محلول، یک رشته DNAی جدید را در جهت َ5 به َ3 و در مقابل رشته های الگو میسازد.مدت زمان این مرحله نیز باید متناسب با نوع DNA پلیمراز و طول رشته DNA باشد. در دمای بهینه، DNA پلیمراز در هر دقیقه، یک هزار باز را پلیمریزه مینماید. در مرحله طویل شدن در صورت وجود سوبسترای کافی و تامین شرایط بهینه، مقدار DNA در محلول PCR دو برابر میشود. بنابر این در هر سیکل PCR، غلظت DNA بصورت تصاعدی افزایش می یابد.
5. مرحله طویل شدن نهایی (Final elongation): این مرحله، پس از آخرین سیکل PCR، به مدت 5 الی 15 دقیقه در دمای 70 الی 74 درجه انجام میشود، تا اطمینان حاصل شود که همه تک رشته های DNA همانند سازی شده اند.
6. نگهداری نهایی (Final hold): در این مرحله، محلول نهایی به مدت کوتاهی در دمای 4 الی 15 درجه قابل نگهداری است.
7. الکتروفورز در ژل آگارز: نهایتا میتوان محصولات PCR را بر روی ژل آگارز و همراه با مارکر وزن مولکولی(DNA lader که حاوی قطعات DNA با اندازه های مشجص است) الکتروفورز نمود، تا صحت انجام PCR بررسی شود.
کاربردهای PCR
1. تشخیص بیماریها: از روش PCR برای بررسی بسیاری از بیماریها استفاده میشود. مثلا در تشخیص بدخیمی هایی نظیر لوسمی (leukemia) و لنفوم (lymphomas)، سنجش PCR مستقیما بر روی DNAی ژنومی انجام میشود تا تغییر در بیان ژنها بررسی گردد. حساسیت این روش ده هزار برابر روشهای معمول است. PCR را میتوان بمنظور شناسائی میکروارگانیسمهایی بکار برد که قابل کشت نیستند و یا سرعت رشد آنها در محیط کشت خیلی کند است از جمله میکوباکتریها (mycobacteria)، باکتریهای غیر هوازی (anaerobic bacteria) و ویروسها (viruses). در مطالعات میکروبیولوژی از روش PCR برای شناسائی عوامل عفونت زا و تشخیص گونه های پاتوژن از غیر پاتوژن نیز استفاده میشود. بدین منظور ژنهای خاصی رهگیری و تعیین مقدار میشوند. بدلیل حساسیت بالای PCR، میتوان بلافاصله پس از عفونت و قبل از ظهور بیماری، وجود میکروارگانیسمها را بررسی و اقدامات درمانی را آغاز کرد.
2. تحقیقات جنایی (forensic analysis): در صحنه جرم، معمولا مقدار DNA بسیار کم است. بنابر این با روش PCR میتوان تکثیر DNA را انجام داد تا مقادیر کافی از مولکولهای ژنتیکی بدست آید. سپس ماهیت DNA بررسی میشود.
3. انگشت نگاری ژنتیک (genetic fingerprinting): با روش PCR میتوان با توجه به ماهیت DNA به هویت اشخاص پی برد. بعنوان مثال والدین را شناسائی کرد و یا رابطه ژنتیکی افراد را بررسی نمود. همچنین رابطه تکاملی موجودات زنده نیز با روش انگشت نگاری ژنتیکی قابل مطالعه است.
4. بررسی DNA قدیمی (ancient DNA): با روش PCR، مولکولهای DNA بسیار قدیمی حتی متعلق به ده ها هزار سال قبل مورد مطالعه قرار گرفته است. مثلا DNA یک ماموت از چهل هزار سال قبل، مومیایی های مصری و تزار روسیه با این تکنیک بررسی شده است.
5. جداسازی DNAی ژنومی: با روش PCR میتوان بخشهایی از DNAی ژنومی را انتخاب و پس از جداسازی تکثیر نمود. مثلا برای کلونینگ DNA و یا تولید شاخصهای دورگه سازی (hybridization probes) در روشهای Southern و Northern، مقادیر زیادی از DNA مورد نیاز است که با روش PCR قابل تهیه است. همجنین در مواردی که حجم نمونه اولیه بسیار کم باشد، با روش PCR میتوان DNAی موجود را تکثیر کرد و سپس مورد مطالعه قرار داد.
6. تعیین توالی DNA (DNA sequencing): پس از تکثیر DNA با روش PCR، میتوان توالی نوکلئوتیدی را تععیین کرد و در صورت لزوم به پلاسمید باکتری یا DNAی کروموزومی در یوکاریوتها الحاق نمود و بدین ترتیب DNAی نوترکیب (recombinant DNA) ایجاد کرد. حتی در مرحله بعد میتوان سریعا با استفاده از PCR، کلنی های باکتری را از نظر وجود این DNAی نوترکیب مورد بررسی قرار داد.
انواع PCR
با ایجاد تغییراتی در تکنیک PCR، زمینه های کاربرد وسیعی ایجاد شده است. بعضی از انواع PCR بطور خلاصه بشرح زیر است:
1. Allele-specific PCR: بمنظور بررسی تغییر در فقط یک نوکلئوتید (single-nucleotide polymorphisms) در تشخیص بیماریها و کلونینگ DNA بکار میرود.
2. Assembly PCR یا (Polymerase Cycling Assembly:PCA): یک روش آزمایشگاهی برای سنتز مولکولهای DNAی بزرگ است. بدین منظور از الیگونوکلئوتیدهایی استفاده میشود که همپوشانی دارند.
3. Asymmetric PCR: در این روش فقط یکی از دو رشته DNA تکثیر میشود. پلی نوکلئوتیدهای حاصل بمنظور تعیین توالی یا تولید شاخص های دو رگه مورد استفاده قرار میگیرند.
4. Helicase-dependent amplification: در این تکنیک برای جدا کردن دو رشته DNA، بجای حرارت از آنزیم هلیکاز (DNA Helicase) استفاده میشود.
5. Hot-start PCR: برای جلوگیری از تکثیر DNAهای ناخواسته مخصوصا در مراحل اولیه PCR استفاده میشود. بدین منظور قبل از افزودن پلیمراز، دمای محلول به نقطه ذوب (مثلا 95 درجه) رسانده میشود.
6. Intersequence-specific PCR: برای انگشت نگاری DNA از طریق تکثیر مناطق بین سکانسهای تکراری بکار میرود.
7. Inverse PCR: کاربرد این تکنیک زمانی است که فقط یک سکانس داخلی شناسایی شده است.
8. Ligation-mediated PCR: در این روش از DNAهای رابط کوچک (small DNA linkers) که به DNAی مورد نظر متصل شده اند، استفاده میشود. کاربرد این روش در تعیین توالی DNA (DNA sequencing)، genome walking و DNA footprinting است.
9. Methylation-specific PCR: این تکنیک توسط Stephen Baylin وJim Herman در دانشکده پزشکی دانشگاه جان هاپکینز ابداع شده است و بمنظور بررسی متیلاسیون در قطعات CpG (CpG islands) در DNAی ژنومیک بکار میرود.
10. Miniprimer PCR: در این روش از یک نوع پلیمراز جدید بنام(S-Tbr) استفاده میشود که قادر است به پرایمرهای کوچک 9 یا 10 نوکلئوتیدی(smalligos) متصل شود. در حالیکه Taq به پرایمرهای بزرگتری متصل میشود که حدود 20 نوکلئوتید دارند. بنابر این با استفاده از S-Tbr، پرایمرهای کوچکتری را میتوان طراحی کرد.
11. Multiplex Ligation-dependent Probe Amplification: در این روش با استفاده از یک جفت پرایمر، میتوان چند نوع DNAی مختلف را تکثیر کرد.
12. Multiplex-PCR: در این تکنیک از چند پرایمر در یک محلول PCR استفاده میشود و آمپلیکونهایی (amplicons) تهیه میشود که اندازه های متفاوتی دارند و مختص DNAهای مختلفی هستند. با هدف قرار دادن چندین ژن در یک محلول PCR، میتوان با آزمایشات کمتر و زمان کوتاهتر، اطلاعات بیشتری جمع آوری کرد.
13. Nested PCR: در این روش از تکثیر DNAی ناخواسته جلوگیری شده اثرات زمینه ای کم میشود. بدین ترتیب در فرآیند تکثیر DNAی هدف، اختصاصی بودن (specificity) افزایش می یابد.
14. Quantitative PCR : این تکنیک برای بررسی وجود DNA، cDNA یا RNA و همچنین تعیین غلظت آنها یکار میرود. یکی از شاخه های مهم این تکنیک Quantitative real-time PCR است که از نظر صحت (accuracy) در بالاترین سطح قرار دارد و در آزمایشگاه های تشخیص بالینی کاربرد وسیعی یافته است. در روش Q-PCR برای تعیین غلظت DNA از رنگهای فلورسانس (نظیر Sybr Green) یا شاخصهای DNAی فلورسانس (نظیر TaqMan) استفاده میشود.
15. RT-PCR: این نوع از PCR بمنظور شناسایی، استخراج یا تکثیر RNA از نمونه های سلول یا بافت مورد استفاده قرار میگیرد. در این تکنیک از ترانس کریپتاز معکوس (reverse transcriptase) برای تبدیل RNA به cDNA استفاده میشود.
16. TAIL-PCR: برای جداسازی سکانس های ناشناخته ای بکار میرود که متصل به یک سکانس شناخته شده اند.
17. Touchdown PCR: یک نوع تغییر یافته از PCR است که موجب کاهش اثرات زمینه ای و غیر اختصاصی میشود. در این روش برنامه PCR به گونه ای طراحی میگردد که در طی سیکل های متوالی، بتدریج دمای مرحله اتصال (Annealing step) کاهش می یابد. بدین ترتیب که در سیکل های ابتدائی، دما در حدود 3 الی 5 درجه بالاتر از Tm پرایمر و در سیکلهای انتهایی در حدود 3 تا 5 درجه پائینتر از Tm پرایمر تنظیم میشود.
18. PAN-AC: در این تکنیک، سلولهای زنده مورد مطالعه قرار میگیرند. به همین دلیل تکثیر DNA در دمای ثابت انجام میشود.