تازه های بیوتکنولوژی
جدیدترین دستاوردهای بیوتکنولوژی، نانوبیوتکنولوژی و بیوانفورماتیک
تازه های بیوتکنولوژی
جدیدترین دستاوردهای بیوتکنولوژی، نانوبیوتکنولوژی و بیوانفورماتیککشف مکانیسم های جدید تنظیم بیان ژن در سلول ها
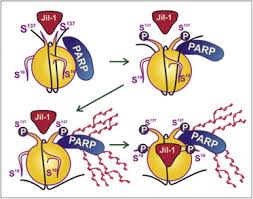
در این سیستم، رشته DNA با ژن هایش در اطراف مولکول های شناخته شده ای به نام هیستون که خودشان به واحد های بزرگتری به نام نوکلئوزوم مونتاژ شده اند، حلقه می شوند. نوکلئوزوم و DNA کروماتین را تشکیل می دهند که ماده اولیه کروموزوم است. این سیستم بسته بندی DNA برای مدیریت توسعه و حفظ سلامتی بسیار حیاتی است. هنگامی که این رویه منحرف بشود، سرطان بوجود می آید.
به گزارش پژوهشکده مجازی بیوتکنولوژی پزشکی، دکتر Alexei V. Tulin(استادیار مرکز سرطان Fox Chase) و همکارانش گزارش کردند که تغییرات شیمیایی نوعی هیستون موسوم به نام H2Av منجر به تغییرات اساسی در شکل نوکلئوزوم می شود و در نتیجه بخش پنهان شده نوکلئوزوم در معرض تماس قرار می گیرد. این بخشی که به تازگی در معرض قرار گرفته است با آنزیم PARP1 میانکنش داشته و آن را فعال می کند.PARP1 به محض فعال شدن، مولکول های شاخه دار طویل پلی (ADP-ribose) را مجتمع می کند، به نظر می رسد این کار برای باز کردن بسته بندی DNA در اطراف جایگاه فعال سازی PARP1 و در معرض قرار دادن ژنهای خاص برای فعال سازی باشد.
به گفته Tulin: در حال حاضر نوکلئوزوم اغلب به عنوان یک توپ کوچک و یا ساختار بی اثر و ثابت به تصویر کشیده می شود. ما دریافتیم که نوکلئوزوم در واقع یک ساختار کاملا پویا است. هنگامی که ما یک هیستون را تغییر می دهیم در واقع کل نوکلئوزوم را تغییر داده ایم.
این مطالعه علاوه بر ارزیابی مجدد نحوه کنترل ژن توسط هیستون ها، یک مکانیسم جدید از تنظیم PARP1 را ارائه کرد. بسیاری از درمان های استاندارد سرطان از جمله داروهای شیمی درمانی و اشعه درمانی به DNA سلول های سرطانی که به سرعت تقسیم می شوند آسیب می زنند، با این حال، اثربخشی این درمان محدود است. تحقیقات نشان داده است که درمان های استانداردی که با داروها همراه است و مانع PARP1 می شود، می تواند سلول های سرطانی را بکشند، اما مهار کننده هایPARP1 در تست آزمایش های بالینی در بیماران مبتلا به سرطان نتایج ناامید کننده ای را بدست آورد. دکتر Tulin می گوید: من باور دارم که شکست های قبلی تا حد زیادی بخاطر یک تصور غلط در مورد نقش PARP1 در سلول های زنده و مکانیزم های تنظیم PARP1 بوده است. حال که ما این مکانیسم تنظیمPARP1 را می شناسیم، می توانیم روشی را برای مهار موثر تراین پروتئین برای درمان بهتر سرطان طراحی کنیم.
تواناییPARP1 برای کنترل فرایندهای سلولی توسط نوکلئوزوم (واحد اصلی بسته بندی DNA که شامل یک بخش از DNA است که در اطراف هشت هسته پروتئین هیستون شبیه به یک رشته ای که بدور قرقره پیچیده شده است، قرار دارد) تنظیم می شود. هیستون ها تحت تغییرات شیمیایی مختلفی قرار می گیرند و نقش مهمی در تنظیم فعالیت ژن ها بازی کند. از طریق این مکانیسم، هیستون ها توانایی PARP1 برای فعال سازی ژن ها و ترمیم آسیب DNAرا کنترل می کنند.
دکتر Tulin می گوید: این مکانیزم تنظیم PARP1 توسط هیستون ها هنوز بسیار جدیداست. محققین معتقدند که PARP1 به طور عمده از طریق تعامل با DNA فعال شده است اما ما ثابت کردیم که مسیر اصلی فعال سازی PARP1 از طریق میانکنش با نوکلئوزوم است.Tulin و همکارانش در مطالعه جدید مجددا چگونگی فعال سازی PARP1 را توسط تغییرات در نوکلئوزوم بررسی کردند. آنها دریافتند که اضافه شدن گروه فسفات به هیستون H2Av باعث تغییر شکل کل نوکلئوزوم و موجب در معرض قرار گرفتن بخش هایی از نوکلئوزوم می شود که پیش از این پنهان بوده است و این کار منجر به برقراری ارتباط و فعال شدن PARP1 می شود.
در حال حاضرTulin و تیم اش برای پیگیری این یافته ها، در حال توسعه نسل بعدی از مهار کننده هایPARP1 هستند. در مقایسه با مهارکننده های PARP1 که در حال حاضر در مطالعات بالینی مورد استفاده قرار می گیرند، این مهار کننده های جدید به طور خاص PARP1 را مورد هدف قرار می دهند.
ما انتظار داریم که مهار کننده های PARP1 هدف قرار گرفته ما در کشتن سلول های سرطانی موثر تر باشد.Tulin می گوید: به همین دلیل، ما معتقدیم که مهار کننده های خاص ما امید های بزرگی را برای درمان سرطان بوجود آورده است.
منبع:
Colin J. Thomas, Elena Kotova, Mark Andrake, Jared Adolf-Bryfogle, Robert Glaser, Catherine Regnard, Alexei V. Tulin. Kinase-Mediated Changes in Nucleosome, Conformation Trigger Chromatin Decondensation via Poly (ADP-Ribosyl)ation. Molecular Cell, 2014; DOI: 10.1016/j.molcel.2014.01.005
منبع: vimb